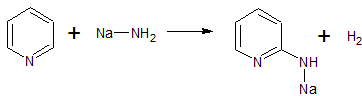Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
пиридин
Синонимы и иностранные названия:
pyridine (англ.)
Тип вещества:
органическое
Внешний вид:
бесцветн. жидкостьБрутто-формула (по системе Хилла для органических веществ):
C5H5NМолекулярная масса (в а.е.м.): 79,11
Температура плавления (в °C):
-41,8Температура кипения (в °C):
115,3Растворимость (в г/100 г растворителя или характеристика):
аммиак жидкий: смешивается [Лит.]
ацетон: растворим [Лит.]
бензол: растворим [Лит.]
вода: смешивается [Лит.]
диэтиловый эфир: смешивается [Лит.]
монохлорид иода: растворим [Лит.]
сульфолан: смешивается [Лит.]
фтороводород: легко растворим [Лит.]
хлороформ: растворим [Лит.]
этанол: смешивается [Лит.]
Плотность:
0,9819 (20°C, г/см3, состояние вещества - жидкость)
Вкус, запах, гигроскопичность:
запах: неприятный
Некоторые числовые свойства вещества:
Порог восприятия запаха в воздухе (мг/л): 0,0002-0,003
Используется для синтеза веществ:
4,4'-дипиридил - вода (1/2)
N-бензоилпиперидин
Реакции вещества:
- Нитруется оксидом азота(V) в диоксиде серы с образованием 3-нитропиридина.. (выход 68%) [Лит.]
- Нитруется смесью азотной кислоты и трифторуксусного ангидрида с образованием 3-нитропиридина. (выход 83%) [Лит.]
- Нитруется нитратом калия в 18% олеуме при 330 С в течение 1 часа с образованием 3-нитропиридина. (выход 15%) [Лит.]
- Ацетофенон реагирует с иодом в растворе пиридина с образованием иодида N-фенацилпиридиния. [Лит.1]
C6H5COCH3 + I2 + 2C5H5N → [C6H5COCH2NC5H5]I + C5H5NHI
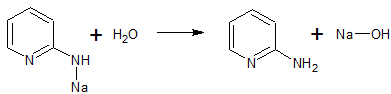
- Пиридин реагирует с амидом натрия в диметиланилине при 100-115 С с образованием 2-аминопиридина (после гидролиза). Выход 75-85%. [Лит.1]
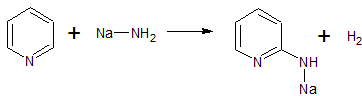
- 1-Метил-2-пиридон может быть получен образоткой пиридина диметилсульфатом с дальнейшим окислением метилсульфата N-метилпиридиния гексацианоферратом(III) калия в щелочной среде. Выход 65-70%. [Лит.1]
- Смесь тионилхлорида с пиридином в отношении 3:1 (об/об) растворяет золото со скоростью 0,3 моль/(м2*ч) (быстрее цианидного и иодидного растворов), также эта смесь растворяет серебро и палладий. [Лит.1, Лит.2]
- Натрий реагирует с пиридином с образованием промежуточного соединения, которое при температуре кипения пиридина дает 2-пиридилнатрий (36%) и 4-пиридилнатрий (56%). [Лит.1]
Реакции, в которых вещество не участвует:
- Не реагирует с оксидом селена(IV) при кипячении. [Лит.]
- Пиридин не реагирует по Фриделю-Крафтсу с образованием алкилпиридинов. [Лит.1]
Показатель преломления (для D-линии натрия):
1,5095 (20°C)
Давление паров (в мм рт.ст.):
10 (13,2°C)
100 (57,8°C)
200 (75°C)
600 (95,6°C)
Показатели диссоциации:
pKBH+ (1) = 5,23 (25°C, вода)
pKBH+ (1) = 4,48 (20°C, формамид)
Индекс удерживания для газовой хроматографии:
739,1 (фаза колонки - DB-5, со скоростью подъема температуры 6 К/мин)
738 (фаза колонки - OV-101, 110°C)
Диэлектрическая проницаемость:
12,3 (25°C)
Дипольный момент молекулы (в дебаях):
2,19 (20°C)
Динамическая вязкость жидкостей и газов (в мПа·с):
0,974 (20°C)
Поверхностное натяжение (в мН/м):
38 (20°C)
Стандартная энтальпия образования ΔH (298 К, кДж/моль):
100,2 (ж)Стандартная мольная теплоемкость Cp (298 К, Дж/(моль·K)):
132,7 (ж)Энтальпия кипения ΔHкип (кДж/моль):
35,54Температура воспламенения на воздухе (°C):
23,3Теплота сгорания (кДж/моль):
2868,1Стандартная энтальпия образования ΔH (298 К, кДж/моль):
140,4 (г)Критическая температура (в °C):
346,8Критическое давление (в МПа):
5,63Источники информации:
- Dictionary of organic compounds. - Vol. 3, naphthacarbazole - zygadenine. - М.: ИИЛ, 1949. - С. 552-553
- Seidell A. Solubilities of organic compounds. - 3ed., vol.2. - New York: D. Van Nostrand Company, 1941. - С. 286-290
- Вредные вещества в промышленности: Справочник для химиков, инженеров и врачей. - 7-е изд., Т.2. - Л.: Химия, 1976. - С. 444
- Некрасов Б.В. Основы общей химии. - Т.1. - М.: Химия, 1973. - С. 556
- Рабинович В.А., Хавин З.Я. Краткий химический справочник. - Л.: Химия, 1977. - С. 173, 225
- Справочник по растворимости. - Т.1, Кн.1. - М.-Л.: ИАН СССР, 1961. - С. 411-412
- Химия: справочное руководство. - Под ред. Гаврюченкова Ф.Г., Курочкиной М.И. и др. - Л.: Химия, 1975. - С. 372-375
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер