
Циклооктин - низший карбоциклический ацетилен, устойчивый при комнатной температуре. 3,3,7,7-Тетраметилциклогептин при комнатной температуре димеризуется в течение нескольких часов, в то время как 3,3,6,6-тетраметил-1-тиациклогептин-4 устойчив даже при 140°С.
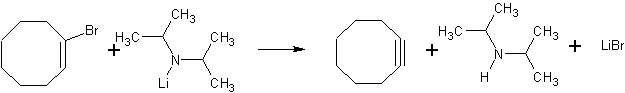
К раствору 4,44 г (51,0 ммоль) диизопропиламина (перегнанного в атмосфере азота над гидридом кальция, т. кип. 84°С/760 мм. рт. ст.) в 20 мл безводного тетрагидрофурана в атмосфере азота при —25°С и перемешивании прибавляют 28 мл (50,4 ммоль) 1,8 М раствора н-бутиллития в гексане. Далее реакционную смесь при этой же тем¬пературе перемешивают еще в течение примерно 30 мин, а затем прибавляют 18,9 г (100 ммоль) 1-бромциклооктена. Следует полностью исключить присутствие воды. Реакционную смесь перемешивают в течение 2,5 ч при медленном нагревании до комн. температуры, выливают в 50 мл 1 М соляной кислоты, охлажденной до 0°С, и экстрагируют пентаном (3 х 40 мл). Объединенные органические фазы дважды промывают насыщенным раствором хлорида натрия и высушивают над сульфатом натрия. После осторожной отгонки пентана остаток фракционируют на маленькой колонке (установка для микроперегонки).
Фракция 1: 3,10 г (56%) циклооктина, т. кип. 48-53°С/15мм рт. ст. n = 1,4873.
Фракция 2: 11,2 г непрореагировавшего 1-бромциклооктена, т. кип. 85-89 С/15 мм.рт.ст.
Впервые получен Домниным в реакции 2-бром-1-хлор-1-циклооктена с металлическим натрием. В 1953 г. он был получен Блюмквистом оксилением α-дигидразона оксидом ртути в присутствии щелочи.
Окисляется на воздухе. С фенилазидом реагирует со взрывом.