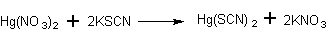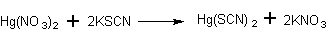Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
ртути(II) тиоцианат
Синонимы и иностранные названия:
mercury(II) thiocyanate (англ.)
ртути(II) роданид (рус.)
Название вещества с нормальным (не справочным) порядком слов русского языка:
тиоцианат ртути(II) Тип вещества:
неорганическое
Брутто-формула (по системе Хилла для органических веществ):
C2HgN2S2Формула в виде текста:
Hg(SCN)2Молекулярная масса (в а.е.м.): 316,75
Температура разложения (в °C):
165Продукты термического разложения:
ртути(II) сульфид; углерода нитрид; углерода дисульфид; Растворимость (в г/100 г растворителя или характеристика):
аммиак жидкий: легко растворим [Лит.]
бензонитрил: мало растворим [Лит.]
вода: 0,055 (20°C) [Лит.]
диоксид серы: 0,02 (0°C) [Лит.]
метиламин: мало растворим [Лит.]
триметиламин: мало растворим [Лит.]
этанол: 0,0494 (20°C) [Лит.]
Метод получения 1:
Источник информации: Ключников Н.Г. Неорганический синтез. - М., 1988 стр. 131
Готовят насыщенный раствор из 7 г нитрата ртути (II), в который, для предупреждения гидролиза, прибавляют небольшое количество азотной кислоты, и раствор из 2 г роданида калия или 1,5 г роданида аммония. Растворы сливают.
Образующийся белый мелкокристаллический осадок отделяют на воронке с отсасыванием, промывают 2-3 раза небольшими порциями воды и высушивают при 50-60°С. При нагревании роданида ртути выше 150°С он разлагается.
Реакции вещества:
- При поджигании спресованного роданида ртути(II) происходит разложение с образованием сульфида ртути(II), нитрида углерода и сероуглерода. Твердые продукты выделяются в виде спека причудливой формы (так называемые фараоновы змеи). [Лит.1]
2Hg(SCN)2 → 2HgS + C3N4 + CS2
Стандартная энтальпия образования ΔH (298 К, кДж/моль)
200,8 (т) [Лит.]
Дополнительная информация::
Реагирует с бромом с образованием родана и бромида ртути.
Источники информации:
- Иванова М.А., Кононова М.А. Химический демонстрационный эксперимент. - М.: Высшая школа, 1969. - С. 44-45
- Ключников Н.Г. Неорганический синтез. - М., 1988. - С. 131
- Справочник химика. - Т. 2. - Л.-М.: Химия, 1964. - С. 184-185
- Химическая энциклопедия. - Т. 4. - М.: Советская энциклопедия, 1995. - С. 587
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер