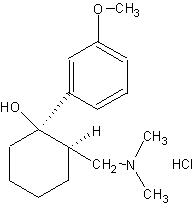

Абсорбция 90%, биодоступность 68% (увеличивается при многократном применении). Метаболизируется в печени путем N- и O-деметилирования с последующей конъюгацией с глюкуроновой кислотой. Выявлено 11 метаболитов, из которых моно-O-десметилтрамадол (M1) обладает фармакологической активностью. Максимальная концентрация в сыворотке крови после приема внутрь капсул - 2 ч, метаболита М1 - 3 ч. Период полувыведения составляет 6 ч (трамадол), 7,9 ч (моно-O-десметилтрамадол), у пациентов старше 75 лет - 7,4 ч (трамадол), при циррозе печени - 13,3 ч (трамадол), 18,5 ч (М1). Выводится почками (25-35% в неизмененном виде), средний кумулятивны показатель почечного выведения 94%. Около 7% выводится с помощью гемодиализа. Проникает через ГЭБ и плаценту, выделяется с грудным молоком (0,1%). Объем распределения 306 л. Связь с белками крови 20%.
Агонист и частичный антагонист опиоидных рецепторов. Обладает центральным действием и действием на спинной мозг (способствует открытию калиевых и кальциевых каналов, вызывает гиперполяризацию мембран и тормозит проведение болевых импульсов). Активирует опиоидные рецепторы (мю-, дельта-, каппа-) на пре- и постсинаптических мембранах афферентных волокон ноцицептивной системы в головном мозге и желудочно-кишечном тракте.
Является рацематом (+) и (-) изомеров, различно участвующих в анальгезирующем действии. Изомер (+) - чистый агонист опиоидных рецепторов, изомер (-) угнетает нейрональный захват норадреналина, активирует центральную нисходящую норадренэргическую систему, что нарушает передачу болевых импульсов и желатиновую субстанцию спинного мозга. Оба изомера действуют синергически.
Болеутоляющее действие начинается через 15-30 мин после приема внутрь и длится 4-6 ч.
В лечебных дозах не влияет на дыхание. Вызывает седативный эффект.
Животные. Снижение двигательной активности, атаксия, экзофтальм, реакция Штраубе, тремор, приступы клонических судорог, угнетение дыхания. Гибель животных обычно наступает в течение первых суток.
Не обладает раздражающим действием и не проникает через нее в количествах способных вызвать признаки отравления. Не обладает эмбриотоксическими, тератогенными и мутагенными свойствами, не влияет на репродуктивную функцию. Наркогенный потенциал и способность к развитию толерантности у трамадола в эксперименте на животных выражена слабо. Кумулятивные свойства выражены слабо. Ccum 10,5 (крысы-самцы, метод Lim et al.) [лит.: Токс. вестник №3 2004].
Человек. Миоз, рвота, коллапс, кома, судороги, угнетение дыхательного центра, апноэ.
При длительном применении возможно развитие лекарственной зависимости. Но при контролируемом применении она развивается крайне редко.
Обеспечение проходимости дыхательных путей, поддержание дыхания и деятельности сердечно-сосудистой системы. Опиатные эффекты могут быть купированы налоксоном, судороги - бензодиазепинами.
Потенцирует действие средств, угнетающих ЦНС (транквилизаторы, седативные и снотворные средства, алкоголь). Индукторы микросомального окисления, в том числе карбамазепин, барбитураты, уменьшают длительность анальгетического эффекта и продолжительность действия. Длительное применение опиоидных анальгетиков или барбитуратов стимулирует развитие перекрестной толерантности. Анксиолитики повышают выраженность анальгетического эффекта.
Налоксон активирует дыхание, устраняя анальгезию после применения опиоидных анальгетиков. Ингибиторы МАО, фуразолидон, прокарбазин, нейролептики повышают риск развития судорог. Хинидин повышает плазменную концентрацию трамадола и снижает концентрацию М1 за счет конкурентного ингибирования коэнзима CYP2D6.
Лекарственное средство: болеутоляющее.