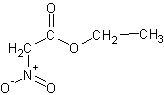

Смесь 50 г (0,38 моль) этилацетоацетата и 25 г уксусного ангидрида при нагревании до 35 С и быстром перемешивании по каплям добавляют в холодную смесь 27 г конц. азотной кислоты и 27 г уксусного ангидрида. Температуру реакционной смеси держат при 32-34 С в процессе всего добавления смеси. Применение сильного наружного охлаждения необходимо если температура поднимается выше этого уровня. После завершения добавления смеси, реакционную смесь выливают в избыток воды с сильным перемешиванием для разрушения избытка уксусного ангидрида. Смесь экстрагирую эфиром и эфирный слой несколько раз промывают водой, затем несколько раз концентрированным раствором карбоната натрия для разрушения нитроацетата. Подкисляют объединенные карбонатные экстракты и выделившееся масло экстрагирую эфиром. Эфирный слой промывают водой, сушат и разгоняют.
Этилнитроацетат собирается при 95-100 С (12 мм.рт.ст.). Выход в виде желтой жидкости 22 г (43%). Дальнейшая очистка основанная на растворении этилнитроацетата в растворе карбоната натрия, выделении его при подкислении и последующей его перегонке дает бесцветный нитроэфир с т.кип. 95-98 С (12 мм.рт.ст.).
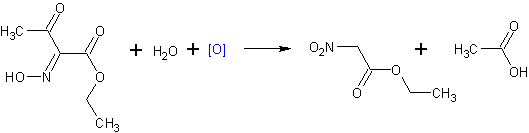
28.5 г (0.18 моля) изонитрозоацетоуксусного эфира помещают в колбу Эрленмейера на 250 мл. При охлаждении водой и непрерывном встряхивании приливают постепенно смесь водного насыщенного раствора 20 г Na2Cr2O7 с 50 мл разбавленной H2SO4 (1 :1). После окончания приливания хромовой смеси реакционную массу встряхивают до перехода желтой окраски в зеленую. Смесь экстрагируют эфиром и эфирный раствор сушат прокаленным сульфатом натрия. После отгонки эфира остающееся масло перегоняют, собирая фракцию кипящую при 75-95 С при 2 мм.рт.ст., из которой при повторной разгонке выделяют 14 г нитроуксусного эфира (58% от теоретич. с учетом изонитрозоацетоуксусного эфира, не вошедшего в реакцию).