Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
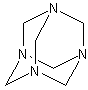
уротропин
Синонимы и иностранные названия:
1,3,5,7-tetraazatricyclo[3.3.1]decane (англ.)
hexamethylenetetramine (англ.)
hexamine (англ.)
methenamine (англ.)
urotropin (англ.)
гексаметилентетрамин (рус.)
гексамин (рус.)
метенамин (рус.)
уризол (рус.)
уротропин (рус.)
Тип вещества:
органическое
Внешний вид:
бесцветн. ромбические кристаллыБрутто-формула (по системе Хилла для органических веществ):
C6H12N4Формула в виде текста:
(CH2)6N4Молекулярная масса (в а.е.м.): 140,19
Температура плавления (в °C):
263Температура разложения (в °C):
280Растворимость (в г/100 г растворителя или характеристика):
амиловый спирт: 2,26 (20°C) [Лит.]
аммиак жидкий: 1,3 (20°C) [Лит.]
ацетон: 0,82 (20°C) [Лит.]
бензол: 0,23 (20°C) [Лит.]
вода: 81,32 (12°C) [Лит.]
вода: 167 (20°C) [Лит.]
глицерин 98,5%: 20,5 (20°C) [Лит.]
диэтиловый эфир: 0,08 (20°C) [Лит.]
ксилол: 0,14 (20°C) [Лит.]
метанол: 9,18 (20°C) [Лит.]
петролейный эфир: не растворим [Лит.]
сероуглерод: 0,13 (20°C) [Лит.]
тетрахлорметан: 0,53 (20°C) [Лит.]
трихлорэтилен: 0,08 (20°C) [Лит.]
хлороформ: 8,09 (12°C) [Лит.]
хлороформ: 9 (20°C) [Лит.]
этанол: 2,89 (20°C) [Лит.]
этанол 90%: 5,58 (20°C) [Лит.]
этанол абсолютный: 3,22 (12°C) [Лит.]
Плотность:
1,331 (-5°C, г/см3, состояние вещества - кристаллы)
1,27 (25°C, г/см3, состояние вещества - кристаллы)
Вкус, запах, гигроскопичность:
вкус: сладкий
запах: без запаха
Некоторые числовые свойства вещества:
Год открытия: 1859 (Бутлеровым)
Способы получения:
- Реакцией формальдегида и аммиака в водном растворе. [Лит.]
Используется для синтеза веществ:
4-гидрокси-3,5-диметоксибензальдегид
Реакции вещества:
- Со слабыми кислотами дает малоустойчивые соли. [Лит.]
- При действии бензил-, аллил- и фенацилгалогенидов дает моноалильные гексаминиевые соли. [Лит.]
- Реагирует с фенолом в присутствии глицеринборной кислоты с образованием 2-гидроксибензальдегида (реакция Даффа). [Лит.]
- При нитровании дымящей азотной кислотой в присутствии нитрата аммония и уксусного ангидрида образует гексоген. [Лит.]
- Выше 200 С начинает разлагаться. При 300 С основными продуктами разложения являются аммиак, метиламин, диметиламин, триметиламин, метан, водород, циановодород. При 800 С циановодород становится основным продуктом распада (94%). [Лит.]
- При действии азотистой кислоты при рН=1 образует 1,3,5-тринитрозогексагидро-1,3,5-триазин. (выход 50%) [Лит.]
- При действии азотистой кислоты при рН=3-4 образует 1,5-эндо-метилен-3,7-динитрозо-1,3,5,7-тетраазациклооктан. (выход 75%) [Лит.]
- Водным раствором серной кислоты количественно гидролизуется до формальдегида и сульфата аммония. [Лит.]
- Образует молекулярный комплекс с сахарозой. [Лит.]
- Реагирует с 1-бутанолом и формальдегидом с образованием трис(бутоксиметил)амина. [Лит.]
- Восстанавливается цинком в кислой или щелочной среде до триметиламина с примесью метиламина и диметиламина. [Лит.]
- Реагирует с циановодородом в присутствии больших количеств кислот с образованием нитрилотриацетонитрила. [Лит.]
- Реагирует с циановодородом в присутствии каталитических количеств кислот с образованием иминодиацетонитрила. [Лит.]
- С ацетилацетоном образует 2,4-диацетил-5-метиланилин. [Лит.]
- С этилацетоацетатом образует смесь диэтиловых эфиров 2,6-диметилпиридин-3,5-дикарбоновой кислоты и 2,6-диметил-1,4-дигидропиридин-3,5-дикарбоновой кислоты. [Лит.]
- При охлаждении насыщенного водного раствора уротропина до 0 С выпадает гексагидрат, который разлагается при 13,5 С. [Лит.]
- При нагревании с анилином при 150-190 С образует 1,3,5-трифенилгексагидро-1,3,5-триазин. [Лит.]
- При действии бензилхлорида и муравьиной кислоты образуется бензилдиметиламин. [Лит.]
- Сиреневый альдегид образуется при реакции 2,6-диметоксифенола с уротропином в смеси глицерина с борной кислотой. Выход 31%. [Лит.1, Лит.2, Лит.3
 ]
] - Реакцией 1,4-диметилбензола с уротропином и трифторуксусной кислотой был получен 2,5-диметилбензальдегид. Выход 55%. [Лит.1]
- С бромом и иодом уротропин дает комплексы C6H12N4 * 2Hal2, теряющие одну молекулу галогена при нагревании или при длительном хранении. [Лит.1]
- С разбавленным спиртовым раствором азотной кислоты уротропин дает мононитрат уротропина, легко растворимый в воде. [Лит.1]
- С 50-60% водным раствором азотной кислоты уротропин дает осадок динитрата уротропина. [Лит.1]
- При кипячении 40 г (0,29 моля) салициловой кислоты с 27 г (0,19 моля) уротропина в 300 мл воды в течении 16 часов образуется смесь 3-формил- и 5-формилсалициловых кислот, которую подкисляют и экстрагируют 3-формилсалициловую кислоту горячим бензолом. Выход 3-формилсалициловой кислоты 7%, 5-формилсалициловой кислоты 16% на салициловую кислоту. [Лит.1]
- Реакцией толуола с уротропином и трифторуксусной кислотой была получена смесь 4-метилбензальдегида (выход 50%) и 2-метилбензальдегида (выход 11%). [Лит.1]
Реакции, в которых вещество не участвует:
- Не реагирует с растворами щелочей. [Лит.]
Стандартная энтальпия образования ΔH (298 К, кДж/моль):
-99,2 (т)Теплота сгорания (кДж/моль):
4212Анализ вещества:
При нагревании с серной кислотой появляется запах формальдегида.
При нагревании с щелочами появляется запах аммиака.
Применение:
Лекарственное средство: антисептик. Отвердитель феноло-формальдегидных смол. Ингибитор коррозии. Фунгицид. Реагент для производства взрывчатых веществ.
История:
Впервые синтезирован Бутлеровым А.М. в 1860 г. из аммиака и полиформальдегида.
Дополнительная информация::
При нагревании улетучивается не плавясь.
Раствор уротропина в уксусной кислоте - мягкий окисляющий агент, используемый для превращения аминов в альдегиды или кетоны.
Источники информации:
- Kaur N., Kishore D. An insight into hexamethylenetetramine: a versatile reagent in organic synthesis / Journal of the Iranian Chemical Society. - 2013. - Vol. 10, No. 6. - С. 1193-1228
- Seidell A. Solubilities of organic compounds. - 3ed., vol.2. - New York: D. Van Nostrand Company, 1941. - С. 434
- Smolin E.M., Rapoport L. s-Triazines and derivatives. - New York: Interscience Publishers Inc., 1959. - С. 545-591
- The Merck Index 11th ed., Merck & Company, 1989. - С. 941
- Государственная фармакопея СССР. - 10-е изд. - М.: Медицина, 1968. - С. 351-352
- Огородников С.К. Формальдегид. - Л.: Химия, 1984. - С. 105 (растворимость в органических растворителях)
- Орлова Е.Ю. Химия и технология бризантных взрывчатых веществ. - Л.: Химия, 1973. - С. 502-503
- Рабинович В.А., Хавин З.Я. Краткий химический справочник. - Л.: Химия, 1977. - С. 187
- Справочник по растворимости. - Т.1, Кн.2. - М.-Л.: ИАН СССР, 1962. - С. 1468
- Химическая энциклопедия. - Т. 1. - М.: Советская энциклопедия, 1988. - С. 507
- Химический энциклопедический словарь. - Под ред. Кнунянц И.Л. - М.: Советская энциклопедия, 1983. - С. 122
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер