Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
магний
Синонимы и иностранные названия:
magnesium (англ.)
Тип вещества:
неорганическое
Внешний вид:
серебристо-бел. гексагональные кристаллы металлаБрутто-формула (по системе Хилла для органических веществ):
MgФормула в виде текста:
MgМолекулярная масса (в а.е.м.): 24,31
Температура плавления (в °C):
650Температура кипения (в °C):
1095Растворимость (в г/100 г растворителя или характеристика):
аммиак жидкий: не растворим [Лит.]
вода: не растворим (20°C) [Лит.]
вода: реагирует (100°C) [Лит.]
гидразин: не растворим [Лит.]
натрий расплавленный: практически не растворим (97,5°C) [Лит.]
натрий расплавленный: растворим (638°C) [Лит.]
ртуть: 0,24 (18°C) [Лит.]
хлорид магния расплавленный: 0,28 (800°C) [Лит.]
хлорид магния расплавленный: 0,41 (1100°C) [Лит.]
Плотность:
1,74 (20°C, г/см3, состояние вещества - кристаллы)
1,57 (651°C, относительно воды при 4°C, состояние вещества - жидкость)
Некоторые числовые свойства вещества:
Год открытия: 1808 (Дэви Г.)
Критическая температура сверхпроводимости (атмосферное давление, массивные образцы, в К): 0,0005
Нормативные документы, связанные с веществом:
- ПНД Ф № 14.1:2:4.135-98 издание 2005 г. "Методика выполнения измерений массовой концентрации металлов методом атомно-эмиссионной спектроскопии с индуктивно-связанной плазмой в питьевой, природной и сточной водах и атмосферных осадках." (Описание документа: Анализ вод методом ICP.)
Способы получения:
- Электролиз расплава хлорида магния. [Лит.]
Реакции вещества:
- При нагревании с серой до 500-600 С образует сульфид магния. [Лит.]
Mg + S → MgS
- Загорается на воздухе ослепительным пламенем при нагревании выше 600 °С с образованием оксида магния. [Лит.]
2Mg + O2 → 2MgO
- При нагревании с селеном образует селенид магния. [Лит.]
Mg + Se → MgSe
- При нагревании с теллуром образует теллурид магния. [Лит.]
Mg + Te → MgTe
- Реагирует с водородом при 570 °С и давлении около 20 МПа в присутствии иодида магния с образованием гидрида магния. [Лит.]
Mg + H2 → MgH2
- При комнатной температуре растворяется в водных растворах солей аммония. [Лит.]
Mg + 2NH4Cl + 2H2O → MgCl2 + 2NH3 · H2O + H2
- Легко растворяется в разбавленной соляной кислоте с образованием хлорида магния и водорода. [Лит.]
Mg + 2HCl → MgCl2 + H2
- Самопроизвольно загорается во влажном хлоре. [Лит.]
- Реагирует с иодметаном в эфирном растворе с образованием метилмагнийиодида. [Лит.]
- При нагревании реагирует с этанолом. Если предварительно магний обработать иодом, реакция идет почти также активно как с водой. [Лит.]
- Тщательно очищенный магний в запаянной ампуле реагирует с ртутью и аммиаком с образованием интеркалята Mg(NH3)6Hg22. [Лит.]
- При 340 С начинает реагировать с хлором с образованием хлорида магния. Реакция протекает легко и до конца. [Лит.]
- Реагирует с хлороводородом в абсолютном этаноле с образованием сольвата хлорид магния - этанол (1/6), который при нагревании в вакууме при 200 С распадается на безводный хлорид магния и этанол. [Лит.]
- Медленно реагирует с жидким аммиаком в присутствии иодида натрия с образованием амида магния. [Лит.]
- Легко растворяется в разбавленной уксусной кислоте. [Лит.]
- Легко растворяется в разбавленной серной кислоте. [Лит.]
- Магний реагирует с горячей водой и водяным паром с выделением водорода и образованием гидроксида магния. [Лит.1]
Mg + 2H2O → Mg(OH)2 + H2
- Азот реагирует с магнием при 300 С с образованием нитрида магния. [Лит.1]
3Mg + N2 → Mg3N2
- Магний реагирует с концентрированной (68%) азотной кислотой с образованием нитрата магния, преимущественно оксида азота(IV) и воды. [Лит.1]
Mg + 4HNO3 (68%) → Mg(NO3)2 + 2NO2 + 2H2O
- Нейтральные растворы персульфата калия растворяют железо, цинк, кадмий, алюминий, магний, кобальт, медь, ртуть с образованием сульфатов. [Лит.1]
- Металлический уран может быть получен восстановлением гексахлороураната(IV) цезия магнием в расплавленной смеси хлорида цезия и хлорида магния при 550 С. Уран отделяется от расплава фильтрацией. Анализ показал, что полученный уран не содержит цезия и магния. [Лит.1]
Реакции, в которых вещество не участвует:
- Не реагирует с холодной водой. [Лит.]
- На холоду не реагирует с плавиковой, концентрированными серной и азотной кислотами. [Лит.]
- Устойчив к разбавленным водным растворам щелочей вплоть до кипения щелочи. [Лит.]
- Не растворяется в водных растворах аммиака. [Лит.]
- Нитрозилхлорид не реагирует с магнием даже при 100 С. [Лит.1]
Периоды полураспада:
2012Mg = 90 мс (β+ (100%))
2112Mg = 122 мс (β+ (100%))
2212Mg = 3,857 с (β+ (100%))
2312Mg = 11,317 с (β+ (100%))
2412Mg = стабилен (дефект масс -13933,567 кэВ (содержание в природной смеси изотопов 78,99%))
2512Mg = стабилен (дефект масс -13192,83 кэВ (содержание в природной смеси изотопов 10%))
2612Mg = стабилен ( (содержание в природной смеси изотопов 10,01%))
2712Mg = 9,458 мин (β-)
2812Mg = 20,915 ч (β-)
2912Mg = 1,3 с (β-)
3012Mg = 335 мс (β-)
3112Mg = 230 мс (β-)
3212Mg = 95 мс (β-)
3312Mg = 90,5 мс (β-)
3412Mg = 20 мс (β-)
3512Mg = 70 мс (β-)
Давление паров (в мм рт.ст.):
0,1 (510°C)
1 (602°C)
10 (723°C)
100 (892°C)
Стандартный электродный потенциал:
Mg2+ + 2e- → Mg, E = -2,363 (вода, 25°C)
Удельная теплоемкость при постоянном давлении (в Дж/г·K):
0,983 (25°C)
1,6 (100°C)
1,31 (650°C)
Стандартная энтальпия образования ΔH (298 К, кДж/моль):
0 (т)Стандартная энергия Гиббса образования ΔG (298 К, кДж/моль):
0 (т)Стандартная энтропия вещества S (298 К, Дж/(моль·K)):
32,7 (т)Стандартная мольная теплоемкость Cp (298 К, Дж/(моль·K)):
23,9 (т)Энтальпия плавления ΔHпл (кДж/моль):
9,2Энтальпия кипения ΔHкип (кДж/моль):
131,8Стандартная энтальпия образования ΔH (298 К, кДж/моль):
147,1 (г)Стандартная энтропия вещества S (298 К, Дж/(моль·K)):
148,5 (г)Стандартная мольная теплоемкость Cp (298 К, Дж/(моль·K)):
20,8 (г)Природные и антропогенные источники:
Содержание в атмосфере Солнца 0,02 ат%.
В виде соединений содержится в пищевых продуктах (мг/100 г): масло сливочное 0,4, голубика 7, абрикос мякоть 8, яблоки 9, вода боржоми 10, яйцо куриное 12, апельсины 13, молоко 14, колбасы 15-30, капуста 16, персики 16, манная крупа 18, помидоры 20, свинина 20-27, говядина 22-25, творог 23, картофель 23, макароны 19-25, смородина черная 31, рыба 35-60, морковь 38, бананы 42, изюм 42, сыр 20-50, хлеб 19-60, шоколад 20-60, мясо кальмара 90, борщ с мясом 101, чернослив 102, курага 105, горох 107, урюк 109, гречка 150-200, ядро фундука 172, арахис 202, соя 226, ядра сладкого миндаля 234, ядро кешью 270, подсолнечник 398, кунжут 540.
Применение:
Используется как легкий конструкционный материал. Для катодной защиты металлов от коррозии. Поглотитель кислорода и восстановитель при производстве бериллия, титана, циркония, гафния, урана.
Дополнительная информация::
 Электронная конфигурация атома 1s22s22p63s2.
Электронная конфигурация атома 1s22s22p63s2.
Устойчивость магниевых сплавов к высокой температуре (до 450 С) заметно улучшается при сплавлении с редкоземельными металлами (напр. Pr/Nd) или торием.
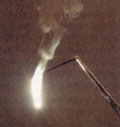
Реагирует с кислотами и солями аммония. Не реагирует с щелочами. Горит на воздухе с ослепительным пламенем (на фото). Горит в углекислом газе и парах воды.
Источники информации:
- Гринвуд Н., Эрншо А. Химия элементов. - Т.1. - М.: БИНОМ. Лаборатория знаний, 2008. - С. 113
- Гурвич Я.А. Справочник молодого аппаратчика-химика. - М.: Химия, 1991. - С. 51
- Девяткин В.В., Ляхова Ю.М. Химия для любознательных, или о чем не узнаешь на уроке. - Ярославль: Академия Холдинг, 2000. - С. 40
- Иванова М.А., Кононова М.А. Химический демонстрационный эксперимент. - М.: Высшая школа, 1969. - С. 47-48
- Корольченко А.Я., Корольченко Д.А. Пожаровзрывоопасность веществ и материалов и средства их тушения. - 2 изд, Ч.2. - М.: Ассоциация Пожнаука, 2004. - С. 40
- Неорганические синтезы. - Сб. 1. - М.: ИИЛ, 1951. - С. 10
- Рабинович В.А., Хавин З.Я. Краткий химический справочник. - Л.: Химия, 1977. - С. 77
- Справочник по растворимости. - Т.1, Кн.1. - М.-Л.: ИАН СССР, 1961. - С. 593
- Физические величины. - Под ред. Григорьева И.С., Мейлихова Е.З. - М.: Энергоатомиздат, 1991. - С. 449
- Эйдензон М.А. Магний. - М.: Металлургия, 1969
- Энциклопедия для детей. - Т.17: Химия. - М.: Аванта+, 2004. - С. 71, 193
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер
 Электронная конфигурация атома 1s22s22p63s2.
Электронная конфигурация атома 1s22s22p63s2.
 Электронная конфигурация атома 1s22s22p63s2.
Электронная конфигурация атома 1s22s22p63s2.